3일전, 29일 아침 메드팩토 백토서팁의 FDA 희귀의약품 지정 뉴스가 떴다.
당일, 그리고 다음날 까지는 FDA페이지에서 검색이 안되다가 오늘 드디어 FDA페이지에 뜬 걸 확인할 수 있었다.
FDA는 매달 ODD지정된 품목을 업데이트한다는 내용을 페이지에서 볼 수 있는 것으로 보아, 10월 1일자로 업데이트 된 것이 아닐까 싶다.

궁금하신 분들은 직접 아래 사이트에서 검색해볼 수 있다.
www.accessdata.fda.gov/scripts/opdlisting/oopd/
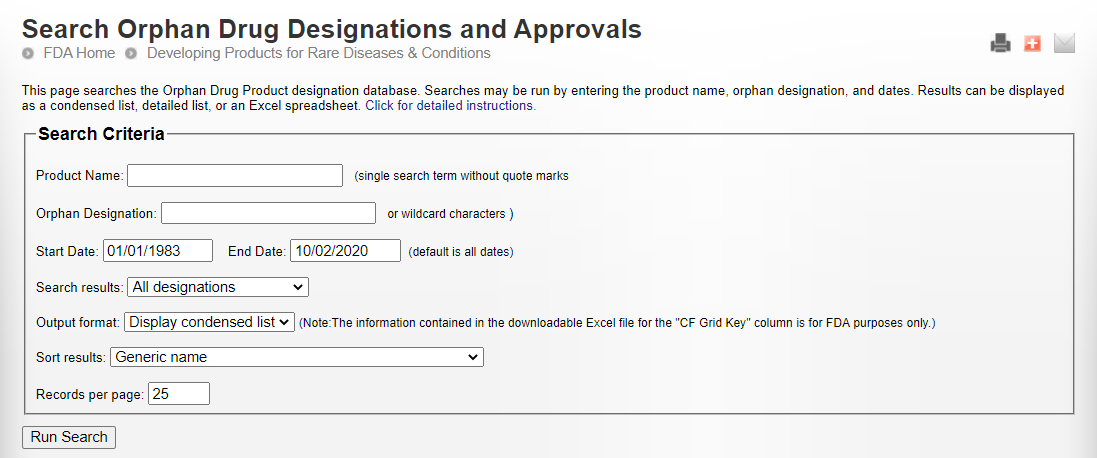
Product name에 vactosertib입력하고 검색 날짜를 9/28이후까지로 지정하여 검색하면 9월 28일자로 지정된 것을 확인할 수 있다. 조금 더 자세한 정보를 확인하면 아래와 같다.

희귀의약품으로 지정되었다는 것은 아래와 같은 혜택을 받는 것을 의미한다.
Orphan Drug Designation Awardees are Granted the Following Benefits from the FDA:
- Tax credits of 50% off the clinical drug testing cost awarded upon approval
- Eligibility for market exclusivity for 7 years post approval
- Waiver of new drug application (NDA)/ biologics license application (BLA) application fee (approximately $2.2 million value) (more details)
1) 임상시험비의 50% 세액공제
2) 승인 후 7년간 시장 독점
3) 신약승인 심사비용 면제 (약 25억원 정도의 가치..)
아직 승인이 난 것은 아니며, FDA ODD(희귀의약품 지정) 를 받았다해서 미국에서 당장 판매를 할 수 있는 것은 아니다.
다만, 승인을 위한 수 많은 관문에 많은 혜택을 받을 수 있게 된 것이라 보면 된다. 호재인 것은 확실!
지금까지 국내 수많은 기업들이 미국 FDA ODD를 받은 바 있는 것으로 보인다.
한국보건산업진흥원에서 낸 보고서에 따르면 2019년 4월 기준으로 36개 성분, 39건이라 한다.


국내 허가는 희귀의약품에 해당되는 조건의 약제라면 희귀의약품으로 지정받고 정식허가로 전환하는 것이 일반적이며, FDA는 보통 희귀질환 지정 > 신속허가 지정 > 정식 허가 순으로 가게된다.
즉 아직 1b의 포스터 결과만 가지고 희귀질환을 지정한다는 것에서 보아도 알겠지만 해당 결과가 매우 인상적이어서 지정을 받았다기보다는 정말 말 그대로 희귀질환에서의 빠른 약물 개발을 위해 각종 혜택을 제공하기 위함이 더 크다.
위의 표의 많은 약제들을 보면 전임상, 임상1상 승인 단계에서 ODD를 받았다.
데이터가 정말 outstanding한 경우에 받게 되는 것이 신속허가 지정이며, 이는 보통 2상 결과가 나오고 신청하게 된다.
호재인 것은 팩트이나 그 이상으로 행복회로를 돌리는 것은 무리가 있다는게 개인적 생각이다.
'조금씩공부' 카테고리의 다른 글
| [미국주식/미국기업] 일루미나 (illumina) 사업 매출 (0) | 2020.12.29 |
|---|---|
| 항체-약물 접합체 (ADC, Antibody-Drug Conjugate) (0) | 2020.09.30 |
| [SITC 2020] 메드팩토 백토서팁 관련 미국면역항암학회 일정 (0) | 2020.09.23 |
| [ESMO 2020] 메드팩토 백토서팁(Vactosertib) ESMO - 위선암, phase 1b 결과 포스터 발표 (0) | 2020.09.20 |
| [ESMO 2020] 리보세라닙/캄렐리주맙 ESMO - 2상 간암 (RESCUE) 포스터발표 (0) | 2020.09.20 |



